Анемии. Патогенетическая классификация
Уменьшение количества эритроцитов и содержания гемоглобина ниже стандартных величин называется анемией. Анемии являются не самостоятельным заболеванием, а симптомом, который сопровождает многие физиологические и патологические процессы и относительно редко вызывается первичными заболеваниями кроветворной системы.
По значениям гематокрита анемии можно разделить по следующим степеням тяжести:
• легкая анемия 36—42 %;
• средняя 24—35 %;
• тяжелая менее 24 %.
Гематокрит менее 15 % — требует экстренного переливания донорской крови.
Патогенетическая классификация (7) Анемии вследствие кровопотери
• острая постгеморрагическая анемия;
• хроническая постгеморрагическая анемия.
Анемии, обусловленные недостаточностью эритропоэза (гипопролиферативные)
1. Гипохромные анемии:
• железодефицитная;
• анемии, связанные с нарушением синтеза пор-финов.
2. Нормохромные анемии:
• анемии хронических заболеваний;
• анемии при хронической почечной недостаточности;
• апластические анемии;
• анемии при опухолевых и метастатических поражениях костного мозга.
3. Мегалобластные анемии:
• анемии, обусловленные дефицитом витамина
• фолиеводефицитные анемии.
Анемии вследствие усиленного разрушения эритроцитов (гемолитические анемии)
1. Анемии, обусловленные внеэритроцитарными факторами:
— иммунные гемолитические анемии:
• изоиммунные гемолитические анемии;
• аутоиммунные гемолитические анемии.
Таблица 9
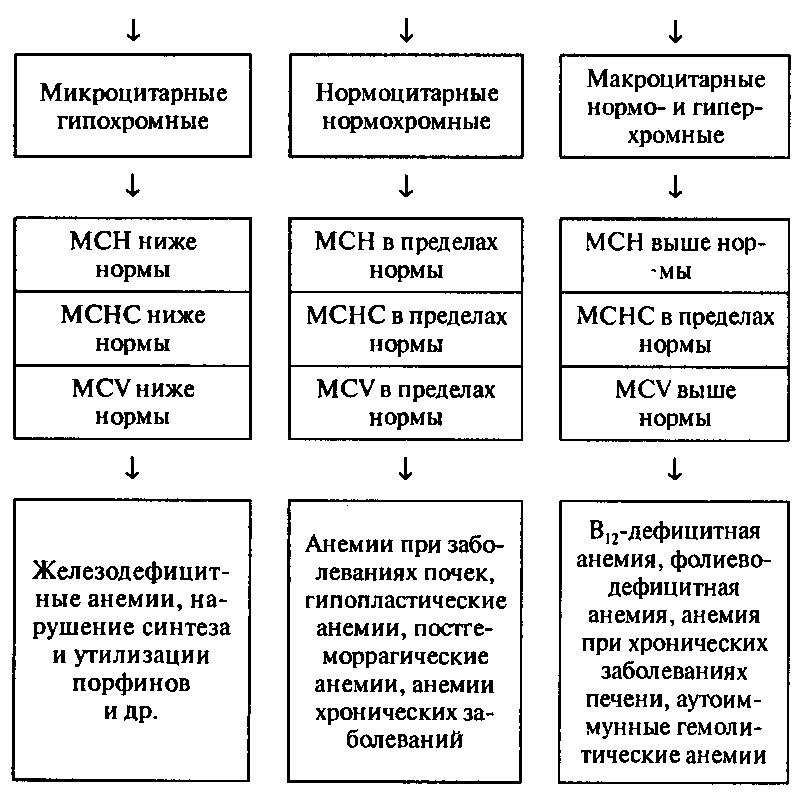
Алгоритм дифференциальной диагностики анемий (М. М. \Vlntrobe)
АНЕМИИ
— гемолитические анемии, обусловленные механическим повреждением эритроцитов.
2. Анемии, обусловленные эритроцитарными факторами:
— гемолитические анемии, связанные с нарушением структуры мембраны эритроцитов (микросфероцитар-ная, овалоцитарная, стоматоцитарная, акантоцитоз);
— гемолитические анемии, обусловленные дефицитом ферментов эритроцитов (ферментов гликолиза, ферментов пентозофосфатного шунта, ферментов глютати-оновой системы);
— гемолитические анемии, связанные с нарушением синтеза глобина.
3. Гемолитические анемии, обусловленные соматической мутацией клеток-предшественников миело-поэза.
Острая постгеморрагическая анемия
Острая постгеморрагическая анемия — состояние, которое развивается в результате быстрой потери значительного объема крови. Причиной острой кровопотери могут быть: нарушение целостности стенок сосуда вследствие его ранения, поражения патологическим процессом при различных заболеваниях (язва желудка и кишечника, опухоль, патологические роды и др.); изменение проницаемости капилляров (геморрагические диатезы) или нарушение в системе гемостаза. Последствия этих изменений-независимо от причин, вызвавших его, однотипны.
Нормальная реакция организма на кровопотерю характеризуется активацией гемопоэза.
Развивающаяся с 1—2-го дня после кровопотери анемия носит нормохромный характер: ЦП близок к 1,0. Наибольшие изменения гематологических показателей периферической крови наблюдаются обычно через 4— 5 дней после кровопотери. Эти изменения обусловлены активной пролиферацией костномозговых элементов. Критерием активности кроветворения (эритропоэза) является повышение в периферической крови количества
ретикулоцитов до 2—10 % и более, полихроматофилов (рис. 28). Ретикулоцитоз и полихроматофилия, как правило, развиваются параллельно и свидетельствуют об усиленной регенерации эритрокариоцитов и поступлении их в кровь. Размер эритроцитов после кровотечения несколько возрастает (макроцитоз). Могут появиться эритробласты. Если количество ретикулоцитов к началу второй недели не снижается, это может свидетельствовать о продолжающемся кровотечении.
Степень выраженности анемии диагностируется по показателям НЬ, эритроцитов, ретикулоцитов, обмена железа.
На 5—8-й день после кровотечения обычно наступает умеренный лейкоцитоз (в 1,2—1,8 раза) и незначительный палочкоядерный сдвиг. Стойкий лейкоцитоз имеет место при наличии присоединившейся инфекции. Количество тромбоцитов увеличивается в 1,5—2 раза.
При небольших кровопотерях депонированное железо поступает в костный мозг, где расходуется для синтеза гемоглобина. Степень повышения сывороточного железа зависит от уровня резервного железа, активности эритропоэза и концентрации трансферрина плазмы. При однократной острой кровопотере отмечается преходящее снижение уровня сывороточного железа в плазме. При больших кровопотерях сывороточное железо остается низким. Дефицит резервного железа сопровождается си-деропенией и развитием железодефицитной анемии. На степень анемии оказывают влияние объем и темп кро-вопотери, время с момента кровотечения, резерв железа в органах депо, исходное количество эритроцитов и гемоглобина.
Гипоксия тканей, развивающаяся при кровопотере, приводит к накоплению в организме недоокисленных
продуктов обмена и к ацидозу, который первое время носит компенсированный характер. Прогрессирование процесса сопровождается развитием некомпенсированного ацидоза со снижением рН крови. В терминальной стадии к ацидозу присоединяется алкалоз. Возрастает дыхательный коэффициент. Развивается гипергликемия, повышается активность ферментов ЛДГ и ACT, что подтверждает поражение печени и почек. В сыворотке уменьшается концентрация Na и Са, увеличивается содержание К, Mg, неорганического Р и С1, концентрация последнего зависит от степени ацидоза и может снижаться при его декомпенсации.
Хроническая постгеморрагическая анемия
Хроническая постгеморрагическая анемия — это ги-похромно-нормоцитарная анемия, возникающая при длительной умеренной кровопотере.
Такие состояния аналогичны железодефицитной анемии (ЖДА) и сопровождают:
• хронические желудочно-кишечные кровотечения;
• воспалительные процессы в матке;
• кровопотери из мочевых путей.
Дефицит железа возможен при несбалансированном искусственном питании и инфекциях молодняка, в результате нарушения всасывания в кишечнике (после обширной резекции тонкой кишки, при хроническом энтерите, лямблиозе, глистных инвазиях).
Нарушение транспорта железа из депо к эритрону имеет место при отсутствии синтеза трансферрина, а также заболеваниях печени, сопровождающихся нарушением белоксинтетической функции (гепатиты, цирроз, рак печени).
Терапия рекомбинантным эритропоэтином приводит к стимуляции эритропоэза и усиленному потреблению железа эритрокариоцитами, что способствует развитию ЖДА-
Таблица 10
Анемии вследствие кровопотери
|
Вид анемии |
Острая постгеморрагическая анемия |
Хроническая постгеморрагическая анемия (ЖДА) |
|
Причины |
Быстрая потеоя зна- |
Длительная умеренная |
|
чительного объема крови: ранение, язва желудка и кишечника, опухоль, патологические роды и др., изменение проницаемости капилляров (геморрагические диатезы) или нарушение в системе гемостаза. |
кровопотеоя: хронические ЖК кровотечения, воспалительные процессы в матке, кровопотери из мочевых путей и др. |
|
|
Характеристики |
Активация гемопоэза: ЦП —1,0, ретикулоциты до 2—10 % и более, поли-хроматофилы, макроци-тоз, снижение НЬ, эритроцитов, MCV, МСН, МСНС в норме. При прогрессироиании |
Истошение поолисЬерати-вой активности костного мозга: количество эритроцитов в норме, снижение НЬ, МСН <ЧЦП<0,7, МСНС, МСУ < нижней границы N. гипохромия, анизоцитоз со склонностью к микроцитозу. |
|
процесса: снижение рН крови, гипергликемия, повышение ЛДГ, ACT, К, Mg, Р, С1, уменьшение Na и Са сывороточного железа. |
В каждом случае дефициту железа предшествует в первую очередь истощение его запасов, затем уменьшается транспортное железо, далее — снижается активность железосодержащих ферментов и в последнюю очередь — нарушается синтез НЬ.
При длительном течении ЖДА истощается пролифе-ративная активность костного мозга, возрастает неэффективный эритропоэз, что приводит к уменьшению количества миелокариоцитов, снижению числа эритроцитов, появлению популяции эритроцитов с увеличенным объемом, возможна задержка созревания грануло-цитов.
При осмотре нужно обратить внимание на поиск причин незначительных длительных кровотечений: кровоточивость десен, сильное поражение блохами и др.
Анемии, связанные с нарушением синтеза порфинов (сидеро-бластные анемии)
Анемии этой группы (довольно редко встречаются у животных) обусловлены недостаточной или аномальной утилизацией внутриклеточного железа при синтезе НЬ, несмотря на нормальное или даже повышенное содержание железа в митохондриях эритрокариоцитов. Такие дефекты могут быть связаны с наследственными нарушениями или с приобретенным характером поражения, например в результате отравления свинцом или недостаточности витамина В6. Отличительным признаком этого типа анемий является насыщение организма железом.
Для этой анемии характерны признаки неэффективного эритропоэза, который определяется как анемия с относительной или абсолютной ретикулоцитопенией. Содержание железа в сыворотке значительно повышено.
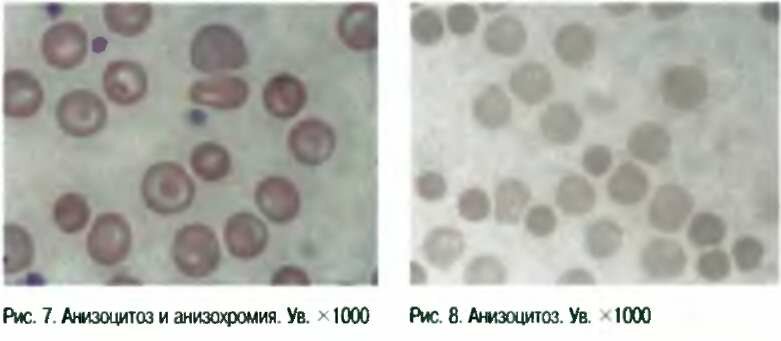
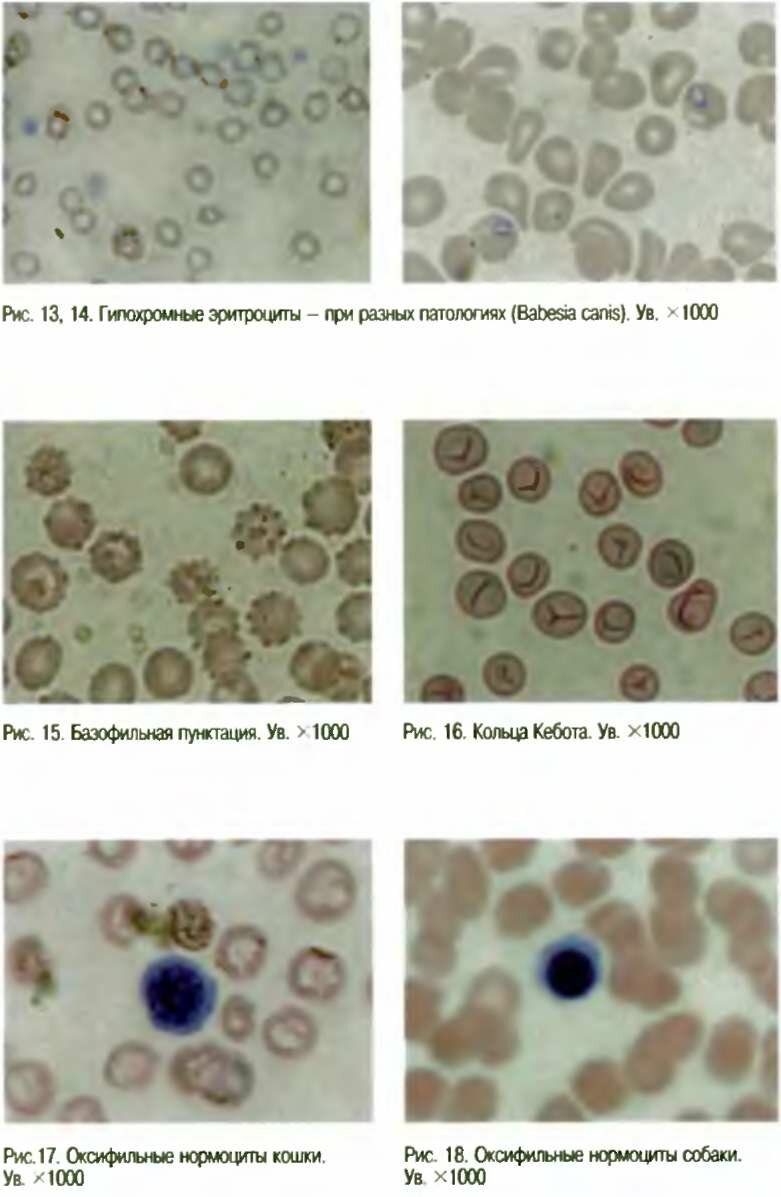
В периферической крови постепенно снижается содержание НЬ в 2 и более раз, эритроциты с выраженной ги-похромией (низкие ЦП, МСН, МСНС), выявляется ани-зо-пойкилоцитоз, появляется базофильная пунктация эритроцитов (рис. 15).
Анемии хронических заболеваний (АХЗ)
Анемии, сопровождающие инфекционные, ревматические и опухолевые заболевания, получили условное название «анемии хронических заболеваний» (АХЗ). Частота их при указанных состояниях достигает 100 %. АХЗ занимают по распространенности второе место после ЖДА. АХЗ характеризуется перераспределительным или функциональным дефицитом железа, вследствие накопления и блокады освобождения железа в тканевых макрофагах, что приводит к снижению доставки железа к эритрокариоцитам костного мозга, нарушению эритро-поэза и развитию анемии.
Чаще анемия при АХЗ носит нормохромный нормо-цитарный, реже умеренно гипохромный характер.
Таблица 11
Дифференциальная диагностика анемии АХЗ и ЖДА
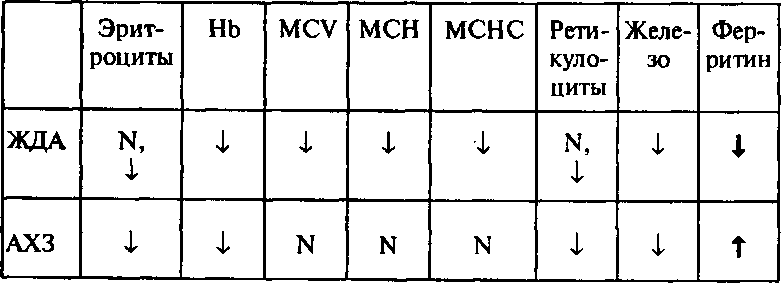
Дифференциальная диагностика истинного и перераспределительного дефицита железа возможна, только при условии определения уровня сывороточного ферри-тина. Ошибочная диагностика ЖДА может повлечь за собой назначение препаратов железа с развитием вторичного гемосидероза.
Анемия при хронической почечной недостаточности
Анемия — один из наиболее характерных синдромов, сопровождающих течение хронической почечной недостаточности (ХПН). При снижении клиренса креатини-на ниже ЗОмл/мин признаки анемии появляются раньше развития выраженной азотемии. Развитие терминальной стадии ХПН проявляется выраженной уремией, сочетающейся с тяжелой анемией.
К причинам, приводящим к развитию анемии, относят:
• дефицит эндогенного эритропоэтина;
• укорочение продолжительности жизни эритроцитов;
• токсическое влияние на эритроциты продуктов азотистого обмена, способствующих мембранолитиче-ским процессам;
• кровопотери, обусловленные дефектом тромбоцитов.
В периферической крови выявляется нормохромная нормоцитарная, реже гипохромная микроцитарная анемия. Количество ретикулоцитов при нефрогенной анемии обычно нормальное или незначительно снижено.
Лечение больных ХПН препаратами рекомбинантно-го эритропоэтина приводит к частичной коррекции анемии, однако вследствие стимуляции эритропоэза может
развиться ЖДА, в соответствии с чем необходимо исследовать параметры метаболизма железа в процессе лечения.
Анемия при хронической почечной недостаточности характеризуется:
• низким гематокритом;
• уменьшенным количеством эритроцитов и содержания в них НЬ;
• уменьшенным количеством ретикулоцитов;
• гипоплазией эритроидных элементов костного мозга.
Выраженность нормоцитарной нормохромной гипо-пластической анемии пропорциональна азотемии (из-за токсического влияния продуктов азотистого обмена).
При б/х анализе крови выявляется: высокий уровень азота мочевины, креатинина, Р, Са, низкий — гидрокарбоната и К, гипопротеинемия, гипоальбуминемия. Содержание железа в сыворотке крови в норме или понижено.
В моче отмечается: нарушение мочеотделения, умеренная протеинурия, наличие активного осадка.
Следует обследовать кошек на носительство вирусов лейкоза и иммунодефицита, чтобы исключить связанную с этими вирусами миелодискразию.
Апластическая анемия
Апластическая анемия (АА) — заболевание, характеризующееся резким угнетением костномозгового кроветворения, торможением процессов пролиферации и дифференцировки клеточных элементов с раз-
витием глубокой панцитопении в периферической крови.
Клиническая картина определяется анемическим и геморрагическим синдромами. Основные проявления АА обусловлены угнетением нормального кроветворения, гипоксией тканей и органов (одышка, тахикардия, слабость) и резкой тромбоцитопенией (кровоподтеки, носовые кровотечения и др.). В результате выраженной нейтропении развиваются пневмония, отит, синусит, пиелит и другие воспалительные процессы, возможен сепсис.
Для периферической крови характерны признаки выраженной нормохромной анемии с резким снижением концентрации НЬ, количества эритроцитов, умеренным анизоцитозом с тенденцией к макроцитозу, пойкилоци-тозу. Содержание ретикулоцитов варьирует от 0,3 до 0,9 %, при гемолизе достигает 4—5 %. Характерным для АА является выраженная лейкопения (до 2,5—0,55 тыс. в мкл.) с абсолютной нейтропенией (8—40 %) и относительным лимфоцитозом. Резко выражена тромбоцитопе-ния, иногда в мазках периферической крови тромбоциты могут отсутствовать. В большинстве случаев АА ускорена СОЭ. К тяжелым формам АА относят случаи с количеством гранулоцитов в крови менее 0,5 тыс. в мкл., тромбоцитов менее 20,0 тыс. в мкл.
Количество эритроцитов и НЬ — снижено, МСУ и МСН — повышено, МСНС — значит повышено.
Исследуются пробы крови на эрлихиоз, вирус лейкоза кошек, на антитела к эритроцитам, лейкоцитам, тромбоцитам, на другие аутоиммунные болезни (антинуклеарные антитела к системной красной волчанке).
Анемии при опухолевых и метастатических поражениях костного мозга
Поражение костного мозга при гемобластозах и множественных метастазах солидных опухолей приводит к угнетению нормальных ростков кроветворения, в том числе и эритроидного, что сопровождается развитием анемии, которая может занимать основное место в клинической картине. Метастазы в костный мозг встречаются при опухолях различных локализаций, однако наиболее характерны для рака молочной железы, предстательной железы, почек, легкого, щитовидной железы, нейробластомы.
Чаще анемия носит нормохромный нормоцитарный характер, количество ретикулоцитов повышено. Нередко развивается панцитопения. В мазках крови выявляется анизоцитоз, пойкилоцитоз, полихромато-филия, встречаются эритрокариоциты. В лейкоцитарной формуле может наблюдаться сдвиг до миелоци-тов. При морфологическом исследовании пунктатов костного мозга выявляются комплексы опухолевых клеток.
Мегалобластные анемии
Анемии, связанные с нарушением синтеза ДНК, могут быть как наследственными, так и приобретенными. Общим признаком этих анемий является наличие в костном мозге мегалобластического кроветворения. При мегалобластных анемиях нарушается синтез нуклеиновых кислот в результате дефицита витамина В^или фо-лиевой кислоты. Сочетанный дефицит их встречается редко, только при нарушении кишечного всасывания.
Чаще наблюдается изолированный дефицит витамина В12, реже — фолиевой кислоты. Причины развития дефицита В]2:
— нарушение всасывания (атрофический гастрит, резекция желудка, поражение тонкого кишечника);
— недостаточное поступление с пищей;
— конкурентное потребление (широкий лентец, использующий В12для собственного роста);
— повышенная утилизация В12 (злокачественные новообразования, гипертиреоз);
— наследственный дефицит транскобаламина-11.
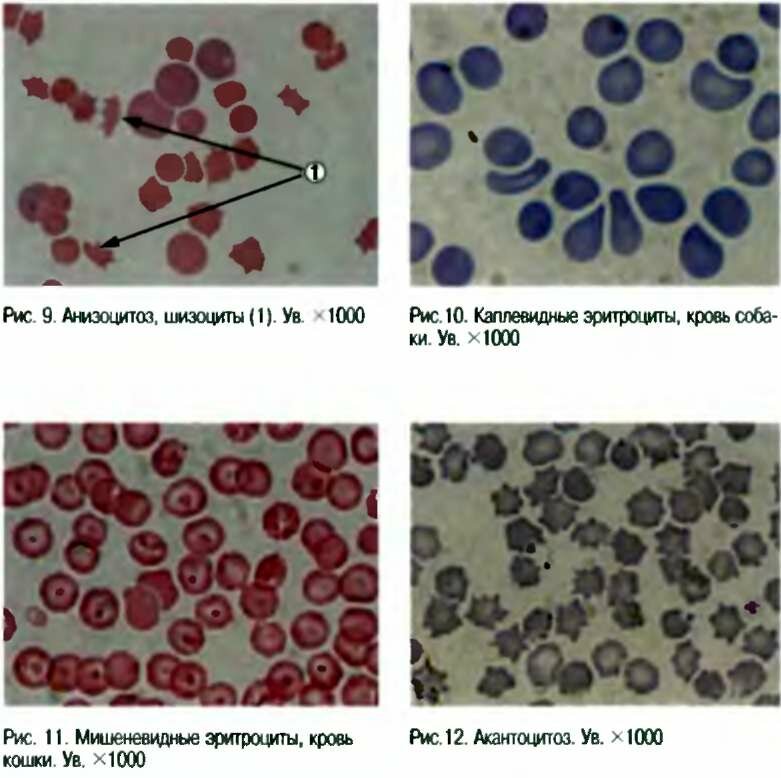
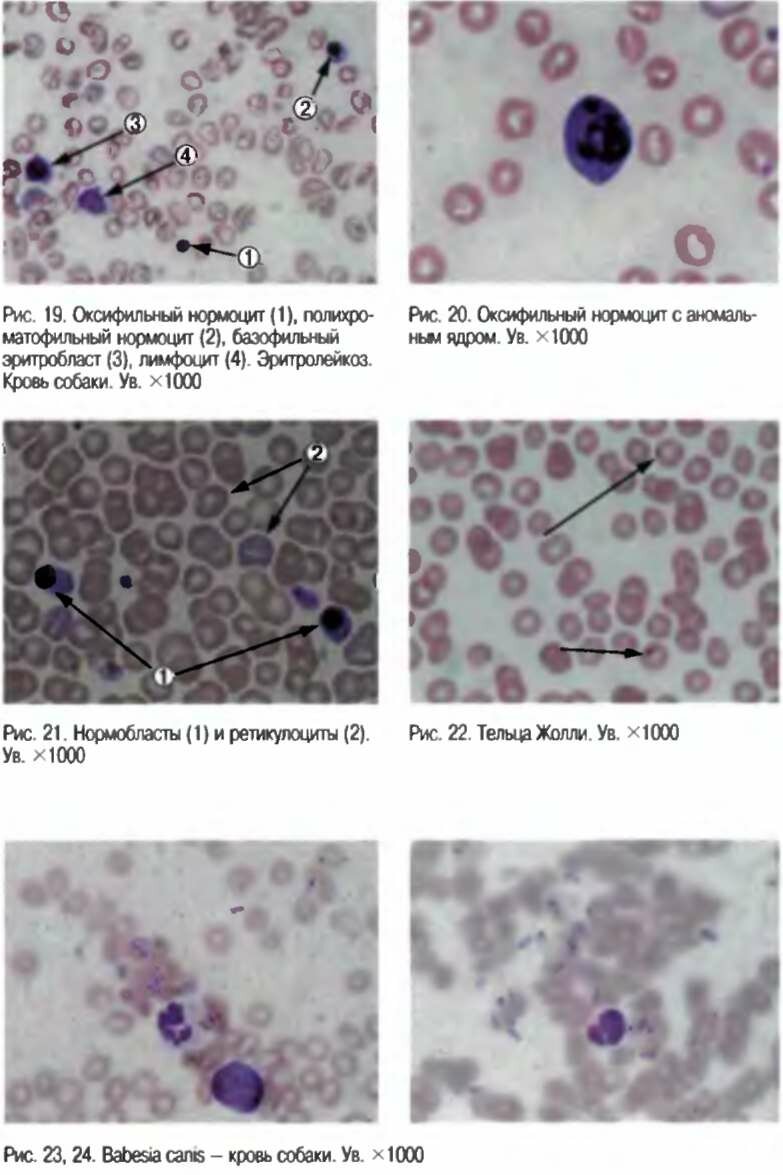
В клиническом анализе крови количество эритроцитов снижается в большей степени, чем уровень НЬ. ЦП больше 1,2. Анемия гиперхромная. Анизоцитоз эритроцитов за счет микроцитов, мегалоцитов. В эритроцитах можно обнаружить тельца Жолли (рис. 22), реже кольца Кебота (рис. 16), встречается базофильная зернистость (рис. 15). Количество ретикулоцитов и лейкоцитов снижено. Отмечается сдвиг лейкоцитарной формулы вправо — появляются крупные полисегментированные ней-трофилы. Уменьшается количество эозинофилов и моноцитов, вплоть до их исчезновения. Относительный лимфоцитоз.
Диагноз В]2-дефицитной анемии может быть установлен только при морфологическом исследовании костного мозга, которое целесообразно проводить до введения витамина В,2. Инъекция В12 в течение 1—2 суток изменяет тип кроветворения в костном мозге.
Гемолитические анемии
Гемолитические анемии — большая группа наследственных и приобретенных заболеваний, при которых
процессы кроворазрушения преобладают над процессами кровообразования. При них снижена продолжительность жизни эритроцитов. Разрушение эритроцитов (гемолиз) может развиться под влиянием эндогенных и экзогенных причин.
К эндогенным причинам относят нарушение структуры гемоглобина и эритроцитов.
К экзогенным — воздействие различных токсических веществ, антител, механических повреждений на эритроциты с неизменными морфологическими свойствами и функциональной активностью.
Продолжительность жизни эритроцитов составляет 90—120 дней. Около 90% состарившихся эритроцитов разрушается в органах ретикуло-эндотелиальной системы (РЭС) преимущественно в макрофагах селезенки и частично в печени, с образованием желчных пигментов, 10 % эритроцитов разрушается в капиллярах сосудистого русла с выделением свободного гемоглобина, который связывается в крови с белком плазмы — гаптоглобином. Комплекс гемоглобин — гаптоглобин поглощается РЭС и разрушается ее клетками. Способность гаптоглобина связывать гемоглобин препятствует экстраренальному его выведению. Превышение резервной гемоглобинсвя-зывающей емкости гаптоглобина или снижение его уровня в крови сопровождается выделением гемоглобина через почки с мочой.
Различают гемолитические анемии с внутриклеточным (эритроциты разрушаются в тканях в результате изменения пластичности) и с внутрисосудистым гемолизом (разрушение внутри сосудов).
Видом гемолиза определеляются симптоматика и лечение заболевания. Каждому виду гемолиза соответствуют определенные лабораторные показатели.
Таблица 12
Сравнительная характеристика внутриклеточного и внутрисосудистого гемолиза
|
Признаки гемолиза |
Внутрисосудистый |
Внутриклеточный |
|
Локализация гемолиза |
Сосудистая система |
РЭС |
|
Патогенетический фактор |
Гемолизины: стрептококки, лептоспи-ры, стафилококки Паоазиты коови: ба-безии, гемобартонел-лы, эрлихии, ана-плазмы Иммунные и аутоиммунные Факторы |
Аномалия формы, неполноценность мембраны, нарушение синтеза НЬ и ферментов |
|
Гепатоспленомегали |
Незначительная |
Значительная |
|
Морфологические изменения эритроцитов |
Анизоцитоз |
Микросфероцитоз, овалоцитоз, мише-невидные и др. |
|
Локализация гемоси-дероза |
Канальцы почек |
Селезенка, печень, костный мозг |
|
Лабораторные признаки гемолиза |
Гемоглобинемия, гемоглобинурия, гемосидеринурия |
Гипербилирубине-мия, повышение стеркобилина в кале и уробилина в моче |
Анемии, обусловленные преимущественно внутри-сосудистым гемолизом, имеют, как правило, острое начало болезни, характеризуются повышением содержания свободного гемоглобина в сыворотке крови, выде-
лением его с мочой и отложением гемосидерина в канальцах почек.
Анемиям, характеризующимся внутриклеточным гемолизом, более свойственно хроническое течение с гемолитическими кризами, ремиссиями и спленомегали-ей, которая развивается в ответ на длительный повышенный гемолиз эритроцитов. Гемолиз с внутриклеточной локализацией процесса сопровождается изменениями обмена желчных пигментов с отложением гемосидерина в селезенке.
Вместе с тем в некоторых ситуациях, например при наличии в крови двух видов антиэритроцитарных антител (агглютининов и гемолизинов), могут обнаруживаться признаки как внутриклеточного, так и внутрисосуди-стого гемолиза. Степень гемолиза зависит от активности клеток РЭС и титра антител.
Сокращение длительности жизни эритроцитов — общая характеристика всех гемолитических анемий. Если интенсивность гемолиза не превышает физиологического уровня, то избыточное разрушение эритроцитов компенсируется регенеративной пролиферацией костного мозга. При этом в крови обнаруживаются признаки активации кроветворения (ретикулоцитоз и полихромато-филия). Ретикулоцитов до 8—10 %, эритроциты и НЬ в норме. Возможны лейкоцитоз и незначительный тром-боцитоз. Другие признаки гемолиза — повышение концентрации неконъюгированного билирубина, гемосиде-ринурия и гемоглобинемия.
При патологическом увеличении разрушения эритроцитов более чем в 5 раз и недостаточной активности гемопоэза развивается анемия, степень которой зависит от интенсивности гемолиза, исходных гематологи-
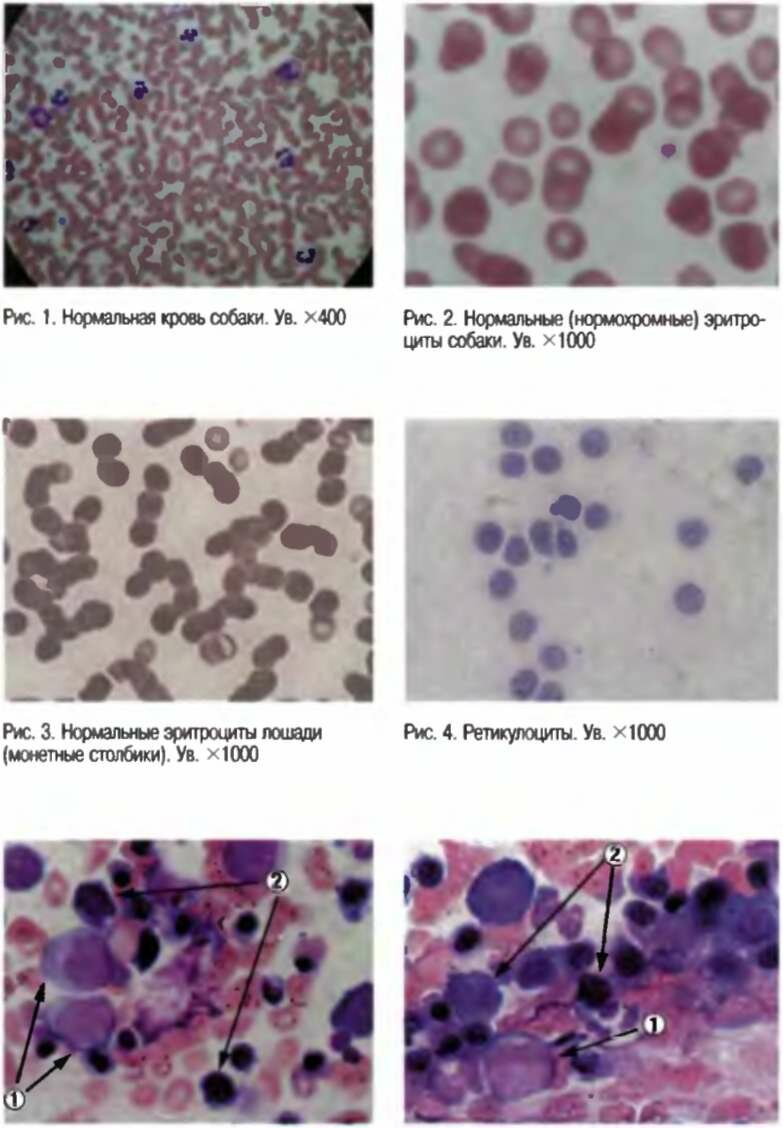
Рис. 5,6. Костный мозг собаки. Клетки: предшественники гранулоцитов (1), предшественники эритроцитов (2). Ув. хЮОО
ческих показателей и состояния эритропоэза. Длительный или часто повторяющийся внутрисосудистый гемолиз приводит к дефициту железа в организме и к развитию ЖДА. В периферической крови наблюдаются ретикулоцитоз, полихроматофилия, эритроноблас-тоз.
Схема лабораторного обследования при гемолитической анемии
1 — прямой тест Кумбса;
2 — поиск паразитов крови (бабезии, гемобартонел-лы, анаплазмы);
3 — поиск иммунных заболеваний путем подсчета тромбоцитов и т. д.;
4 — поиск инфекционных заболеваний, опухолей лимфатической и моноцитарной систем;
5 — сбор анамнеза о принимаемых медикаментах, вакцинах, возможности контакта с ядами;
6 — холодовой или агглютинационный тест;
7 — тест осмотической стойкости эритроцитов. Прямой тест Кумбса используют для выявления им-
муногемолитических анемий, при которых, вследствие большей частью неясных причин, образуются антитела, направленные против собственных эритроцитов (аутоан-титела). Эти полные или неполные антитела и/или комплемент располагаются на поверхности эритроцитов и изменяют при этом их мембрану. Впоследствии происходит агглютинация и/или гемолиз эритроцитов, и они фагоцитируются в РЭС (прежде всего, селезенка) из-за своей измененной поверхности. Встречаются также вторичные иммуногемолитические анемии, например при
красной волчанке, опухолях, лимфопролиферативных заболеваниях, инфекциях, аутоиммунных заболеваниях (тиреоидит, неспецифический язвенный колит, сахарный диабет 1 типа, саркоидоз) и аллергии на медикаменты.
В противоположность к аутоантителам изоантитела воздействуют не на собственные, а на чужие эритроциты. Изоантитела направлены против некоторых групп крови и могут возникать при неправильном переливании крови.
⇐Характеристика функциональной активности эритроцитов || Оглавление || Тромбоциты⇒